De Luchtkwaliteit en Ozon O3
Ozon (O3)wordt niet rechtstreeks uitgestoten, maar wordt gevormd uit stikstofoxiden, vluchtige organische stoffen en koolmonoxide.
De concentratie ozon (O3) is vooral afhankelijk van het weer.
In heel Europa wordt de bevolking gewaarschuwd bij ozonconcentraties boven 180 (μg/m3).
Een concentratie van 240 (μg/m3) is de Europese alarmdrempel.
Ozon (O3) is een gas dat zowel hoog in de atmosfeer, als dicht bij het aardoppervlak voorkomt.
Hoog in de atmosfeer, in de stratosfeer, komt ozon van nature voor en beschermt ons tegen schadelijk UV-licht.
Dicht bij het aardoppervlak ontstaat ozon uit de reactie tussen NOx en zogenaamde vluchtige organische stoffen (VOS). NOx en VOS zijn afkomstig uit natuurlijke bronnen (e.g. bossen, rijstbouw, rundvee) en menselijke activiteiten (verkeer, industriële processen, biomassaverbranding).
Ozon wordt dus niet direct uitgestoten door bijvoorbeeld wegverkeer of industrie. NOx, VOS, en Ozon (O3) zijn stoffen die samen bijdragen aan smogvorming.
Algemene informatie
Ozon (O3) is bij kamertemperatuur en normale druk gasvormig. Als gevolg van het oxiderende effect is het giftig voor de mens (MAK waarde = 0,2 mg / m3). Heftige hoofdpijn is gebruikelijk bij ozon absorptie. Het gas is te ruiken bij hoge concentraties als gevolg van de oxiderende effect op de nasaal karakteristieke prikkels, terwijl het bij lage concentraties reukloos is. De geurdrempel ligt op 40 µg / m3, echter raakt men snel gewend aan de geur en wordt het lastiger om op te merken.
- Vanwege het gevaar voor het organisme moet de ozonconcentratie worden bepaald.
- Ozonmeters hebben een lage responstijd bij hoge gevoeligheid.
- Ozon wordt ook gebruikt voor de sterilisatie bij de behandeling van afvalwater.
- Er zijn niet alleen ozonmeters voor de lucht, maar ook voor het vastleggen van de ozon inhoud van water (fotometer).
Gezondheidseffecten
Acute blootstelling aan ozon kan leiden tot problemen met de luchtwegen zoals moeite met ademhalen. Er zijn aanwijzingen dat ozon verband houdt met sterfte door hart- en vaatziekten.
Hoge blootstelling kan leiden tot astma. Bij langdurige blootstelling is er kans op onherstelbare longschade. Er zijn ook aanwijzingen dat hoge blootstelling leidt tot astma.
Typische concentraties
De concentratie voor ozon varieert van 40-55 ug/m3 met in een groot deel van Nederland een gemiddelde van circa 48 ug/m3. Actuele meetwaarden staan op de website luchtmeetnet.nl.
Wettelijke grenswaarden
Er is een 8-uursconcentratie van 120 µg/m3 die maximaal 25 dagen per jaar overschreden mag worden. Deze norm werd de afgelopen jaren in Nederland niet overschreden.
Meten van ozon
Binnen het Landelijk Meetnet Luchkwaliteit wordt ozon gemeten middels de mate van absorptie van UV-licht.
Eisen voor het meten van ozon
Niet van toepassing.
Ozon en wetenschap
De ontdekking van ozon
Ozon werd ontdekt door Christian Friedrich Schonbein in1840. Werner von Siemens vond de ozongenerator uit, waarmee door elektrostatische ontladingen op industrieële schaal ozon gemaakt kan worden. De naam ozon komt van het Griekse "ozein", wat ruiken betekent. Dit verwijst naar de kenmerkende onaangename geur van het gas.
Ozon maakt een belangrijke component uit van luchtvervuiling, waar het ontstaat in foto chemische smog.
Ozon (stof)
Ozon is een enkelvoudige stof van het element zuurstof, met als brutoformule O3. Bij standaard temperatuur en druk is ozon een kleurloos tot licht blauw gas met een onaangename prikkelende geur. In vloeibare vorm is het donker blauw. Het smeltpunt ligt bij -193 °C en daar onder is ozon een donker blauwe vaste stof. De molecule bezit een gebogen moleculaire geometrie, met een bindingshoek van 116,8°. Ozon is een sterke oxidator. Ozonopwekking gebeurt door middel van een ozongenerator.
Ozon in de atmosfeer
Ozon ontstaat van nature in de atmosfeer onder invloed van elektrische ontladingen (zoals tijdens onweer) en door ultraviolette straling met een golflengte onder 240 nm in de bovenste lagen van de atmosfeer (de stratosfeer).
Toepassingen van Ozon
Ozon werkt desinfecterend en wordt gebruikt om bijvoorbeeld drinkwater te ontsmetten. Het voordeel ten opzichte van bijvoorbeeld dichloor is dat het geen smaak in het water achterlaat. Verder wordt ozon nog ingezet bij het zuiveren van bronwater, zwemvijvers, koi vijvers, zwembaden en van oppervlaktes die in contact komen met voedsel, bij het verwijderen van sporen van gisten uit lucht (belangrijk wanneer voedsel ingepakt wordt), bij het schoonmaken en bleken van stoffen, het ontgeuren van interieurs en materialen na brandschade en bij het verwijderen van ongewenste schadelijke stoffen (bijvoorbeeld herbiciden) uit water. Men past ozontechniek toe op koivijvers, zwembaden, luchtbehandeling en voor het reinigen van vervoersmiddelen, waaronder auto's, boten, caravans, touringcars en kleine vliegtuigen voor commercieel gebruik. Er bestaat professionele zelfoperende ozonapparatuur die kan worden ingezet bij geurbehandeling en stankbestrijding.
Tevens wordt de ozonapparatuur ook ingezet bij stankbestrijding bij brandschades. De roetgeur van de brandschade trekt in de gehele woning, door ozon in de woning toe te passen wordt de brandgeur eenvoudig verwijderd.
In de intensieve visteelt en de aquaristiek wordt ozon als desinfectiemiddel gebruikt en voor afbraak van afvalproducten van de vis. Het wordt ook toegepast als oxidator bij bodemsaneringen (C-sparge) van organische verontreinigingen (bijvoorbeeld BTEX of trichlooretheen).
In de organische synthese wordt ozon aangewend bij de ozonolyse. Deze reactie wordt gebruik om alkenen oxidatief te splitsen. Zo wordt cyclohexeen geoxideerd tot adipaldehyde Het medisch gebruik van ozon komt nog steeds voor, met name in Cuba wordt het toegepast bij kankerbestrijding.
Opwekking ozon
Ozon kan op twee manieren worden opgewekt. Ozon kan doormiddel van UV licht worden opgewekt en doormiddel van corona discharge. Ozongeneratie doormiddel van corona discharge wordt het meest toegpast en biedt het beste rendement en voordelen voor de ozonproductie. Voordelen van de corona discharge zijn onder andere de grotere duurzaamheid van de unit, hogere ozonproductie en qua kosten is het effectiever dan toepassing door middel van UV licht. Een ozongenerator word onderscheiden in de hoeveelheid ozonproductie bijvoorbeeld 1 gram, 2 gram, 3 gram, 4 gram, 5 gram, 6 gram of bijvoorbeeld 10 gram.
Ozonproductie door middel van UV licht kan beter wordt toegpast wanneer de ozon productie klein mag zijn. Het principe van ozonopwekking bij corona discharge bestaat uit de volgende onderdelen: een zuurstof bron, stoffilters, gasdrogers, ozongenrator, contactunits en ozondestructors. In de ozongenerator zit een corona discharge element. Hierin wordt ozon uit zuurstof geproduceerd door het opwekken van een hoge spanning (6-20kV). Over de elektrode wat een elektrische ontlading veroorzaakt ofwel "corona discharge". Deze corona discharge ontleedt het moleculaire zuurstof, door botsing met electronen, tot atomaire zuurstof.
Enkele van deze zuurstof-atomen vormen samen weer een ozon-molecuul. Terwijl andere weer samen gaan tot moleculair zuurstof. Voor de controle van de electrische ontlading en het onderhouden van de “corona”, is er een diëlektrikum aanwezig, uitgevoerd in keramiek of glas. De ozonelektrode zijn vervaardigd uit glas. Glas is slijtvast en kan tegen extreme omstandigheden waaronder; ozon, hoge temperaturen en salpeterzuur.
De meeste ozongeneratoren hoeven niet gekoeld te worden met water, ze zijn vaak luchtgekoeld. Voor de productie van ozon kan omgevingslucht worden gebruikt (aangevoerd door een luchtpomp) of pure zuurstof. Pure zuurstof (100%) is een ideale methode wanneer er een hoge ozonopwekking moet plaatsvinden. Wel is pure zuurstof gevaarlijk omdat brandgevaar kan optreden in het koolfilter. Laat u daarom altijd adviseren over het gebruik met zuurstof als aanvoergas naar de ozongenerator. Het rendement met zuurstof als aanvoergas is tot wel 5 keer groter dan met alleen lucht.
Om deze lucht te conditioneren wordt deze langs luchtdrogers en stoffilters geleid. Zo wordt vochtschade voorkomen aan de ozonelektrode. Ozondestructors zijn bedoeld om het overtollige ozon na gebruik weer af te breken.
De generatie van ozon is erg energie intensief, namelijk ca. 90 % van de energie wordt verbruikt aan produktie van licht, geluid en voornamelijk hitte. Belangrijke factoren van invloed op de ozongeneratie zijn: zuurstofconcentratie inlaat, luchtvochtigheid en zuiverheid van gas (inlaat), temperatuur koelwater en elektrische parameters. Voor het minimaliseren van de gebruikte energie bij een hoge ozon opbrengst is het belangrijk dat deze factoren optimaal zijn.
Toxicologie en veiligheid
Ozon is een toxische verbinding. Het is ongezond om langdurig ozon in te ademen, ook in lage concentraties. Ozon ontleedt bij verwarming in zuurstofgas, hetgeen het brandgevaar verhoogt. Het is een sterke oxidator, die hevig reageert met brandbare en reducerende stoffen. Ozon reageert met alkenen, aromaten zoals aniline, ethers, dibroom, stikstofverbindingen en rubber, waardoor schokgevoelige stoffen ontstaan. Het tast alle metalen aan, behalve de edelmetalen iridium, goud en platina.
Ozon kan in het lichaam worden opgenomen door inademing. Een schadelijke concentratie van dit gas in de lucht zal snel worden bereikt bij het vrijkomen ervan.
Ozon is irriterend voor de ogen en de luchtwegen. Inademing van het gas kan longoedeem veroorzaken en kan op astma lijkende reacties teweeg brengen. Ozon kan effecten hebben op het centraal zenuwstelsel, met als gevolg hoofdpijn, verzwakte waakzaamheid en prestaties.
De luchtkwaliteit ofwel de verwachte concentraties in microgram per kubieke meter (ug/m3) vind u onder ozon maximum uurwaarde
Kopieerapparatuur die met lasertechnieken in plaats van inkt werken en laserprinters produceren ozon. Zij kunnen dan ook het best in een goed geventileerde aparte kamer worden geplaatst.
Structuurformule en molecuulmodel O3
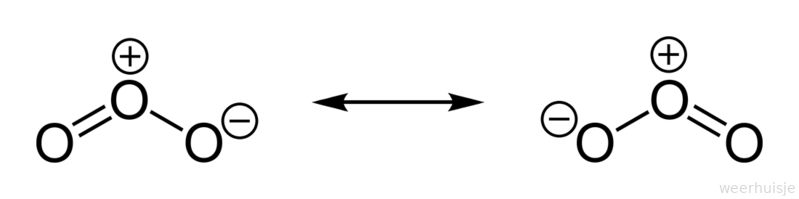
Structuurformule van ozon O3 (als resonantiestructuren)

Molecuulmodel van Ozon O3
 Ozon, opgelost in dichloormethaan
Ozon, opgelost in dichloormethaan
Algemeen
Molecuulformule: O3
IUPAC-naam: ozon
Molmassa: 47,9982 g/mol
SMILES: [O-][O+]=O
InChl: 1/O3/c1-3-2
CAS-nummer: 10028-15-6
EG-nummer: 233-069-2
PubChem: 24823
Beschrijving: Kleurloos tot lichtblauw gas met een prikkelende geur
Waarschuwingen en veiligheidsmaatregelen
 |
 |
 |
Gevaar
H-zinnen
H270 (Kan brand veroorzaken of bevorderen; oxiderend.)
H330 (Dodelijk bij inademing)
H319 (Veroorzaakt ernstige oogirritatie)
H370 (Veroorzaakt schade aan organen)
H372 (Veroorzaakt schade aan organen bij langdurige of herhaalde blootstelling)
[blootstellingsroute vermelden indien afdoende bewezen is dat het gevaar bij andere blootstellingsroutes niet aanwezig is]
EUH-zinnen - geen
P-zinnen
P284 (Adembescherming dragen)
P271 (Alleen buiten of in een goed geventileerde ruimte gebruiken)
P310 (Onmiddellijk een antigifcentrum of een arts raadplegen)
P320 (Specifieke behandeling dringend vereist (zie ... op dit etiket))
P304 (Na inademing: het slachtoffer in de frisse lucht brengen en laten rusten in een houding die het ademen vergemakkelijkt)
P340 (Na inademing: het slachtoffer in de frisse lucht brengen en laten rusten in een houding die het ademen vergemakkelijkt)
P501 (Inhoud/verpakking afvoeren naar ...)
Carcinogeen - mogelijk (IARC-klasse 3)
MAC-waarde - 0,2 mg/m3
Fysische eigenschappen
Aggregatietoestand: gasvormig
Kleur: kleurloos-lichtblauw
Dichtheid: 0,002144 g/cm3
Smeltpunt: -192,5°C
Kookpunt: -111,9°C
Oplosbaarheid in water: 0,57 g/L
Thermodynamische eigenschappen
ΔfG>og - 163,2 kJ/mol
ΔfHog - 142,7 kJ/mol
Sog, 1 bar - 238,93 J/mol-K
Cop,m - 39,29 J/mol-K
WEERHUISKE.nl
Onze 1e website om onze weerdata en gevens te presenteren, online sinds 2012. Tegenwoordig ziet u op deze website de weergegevens van weerdiensten zoals Weeronline en Buienrader.
KLIKWSGB.nl
Onze 2e website om onze weerdata en gevens te presenteren, online sinds 2012. Hier presenteren wij puur onze eigen gegevens en de weersverwachting.
Colandino.nl
Op deze website tonen we de hardware van ons weerstation en geven we ook uitgebeide omschrijvingen en reviews over gebruikte hardware. Onder andere Raspberry Pi, Arduino, Linux, Zelfbouw enz..
KLIK


